硬胶囊剂的质量要求
胶囊剂在制备过程中受微生物污染的机会很多,如空囊壳在运输和存放过程中,在制作填充的整个过程中,内、外包装材料等都会污染微生物。中药全粉制成胶囊剂污染更严重,处理不当,常在存放过程中就出现内容物成轩或成条索。
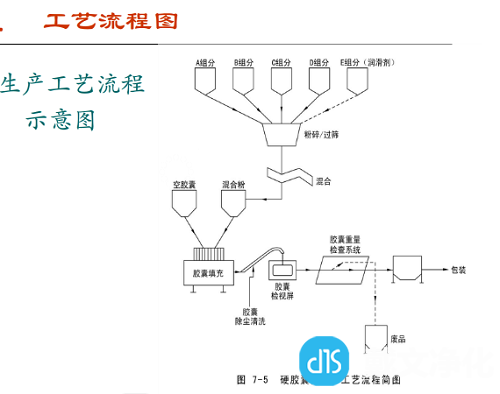
硬胶囊制剂的工艺流程
硬胶囊剂的制备工艺流程通常为: 制备空囊→药物和辅料混合→胶囊的填充与套合→整理→包装→质检→成品, 空胶囊的制备大体经过:溶胶→蘸胶→干燥→拔壳→截割→整理等工序。
胶囊的生产需要按照GMP标准
戴文净化通过制药行业的强性质标准GMP和胶囊的生产工艺流程的深入了解,对胶囊的GMP制药车间提出以下建议:
1,遵循“三协调”原则即人流物流协调、工艺流程协调、洁净级别协调,正确划分生产工艺流程。中生产区域的洁净区别,按工艺流程合理布置,避免生产流程的迂回、往返和人、物流交叉等。
2,胶囊剂分硬胶囊剂、软胶囊剂和肠溶胶囊剂。净化车间硬胶囊剂属口服药剂,其暴露工序,包括拆除包装后开始暴露的原辅料、胶囊、包装材料的准备工序、配料、混合制粒与干燥、充填、灯光、内包装等工序,均应处在30万级环境之中。
3,净化车间软胶囊剂和硬胶囊剂一样能掩盖药物的不良气味、减少刺激性、防止氧化分解以增加药物的稳定性。软胶囊剂生产的所有暴露工序也均应处在30万级的洁净环境中,软胶囊室温除湿用的低湿度空气的洁净度也应当是同一洁净级别。
4,净化车间软胶囊剂的干燥不能在较高温度下进行,因此现行工艺也可以利用恒温恒湿的工艺保持车间温度的稳定,软胶囊的包装形式同于硬胶囊,可以是瓶装,也可以用铝塑泡罩包装。
制药净化工程的原理
气流→初效净化→空调→中效净化→风机送风→管道→超高效净化风口→吹入房间→带走尘埃细菌等颗粒 → 回风百叶窗→初效净化 重复以上过程,即可达到净化目的。
气流方式:顶棚满布高效过滤器送风,格栅地板回风。
制药厂净化工程主要技术参数
室内换气次数:十万级10-15次/小时;万级15-25次/小时;千级50-52次/小时;
百级操作点断面平均风速0.25-0.35m/s。室内噪声:≤65dB(A);
室内压差:高洁净区对相邻的低洁净区≥5Pa、对非洁净区≥10Pa;
室内温度:冬季>16℃±2℃;夏季 <26℃±2℃;(常温)
室内相对湿度:45-65%(RH);(特殊要求)
室内噪声:≤60dB(A);
室内照度:≥300Lux;新风量:总送风量的20%-30%。
结构材料
1、洁净室围护结构的墙面、顶面材料一般采用50mm厚的夹芯彩钢板。
配套净化专用的氧化铝型材制作。门;采用净化密闭门,窗;采用铝合金玻璃固定窗。
2、地面;采用无溶剂环氧自流平洁净地坪或采用高级耐磨PVC洁净地板。
3、净化通风管道;选用镀锌薄钢板外加保温材料制作。
戴文净化提供服务
戴文净化可提供制药,医院,食品,电子,化妆品等多个行业的净化车间的咨询、规划、设计、施工
装修等配套服务。工程的以下部分均可提供
1. 净化装饰工程
2. 地面工程
3. 净化空调与通风系统
4. 冷热源系统工程
5. 照明系统工程
6. 动力系统工程
7. 通信系统工程
8. 监控系统工程
9. 自动化控制系统工程
10. 给排水系统工程
11. 工艺管道系统工程